Metan
Methan (mimo chemii dle PČP metan) neboli podle systematického názvosloví karbanje nejjednodušší alkan, a tedy i nejjednodušší stabilní uhlovodík vůbec. Při pokojové teplotě je to netoxický plyn bez barvy a zápachu, lehčí než vzduch (relativní hustota 0,55 při 20 °C).

Příprava
Hlavním zdrojem methanu je přírodní surovina zemní plyn. Přímá příprava sloučením uhlíku s vodíkem je prakticky nemožná, vzhledem k tomu, že by uhlík musel být nejprve převeden do plynného stavu. Teoreticky však lze methan připravit dvoustupňovou syntézou přes sirouhlík
- C + 2 S → CS2,
který pak reakcí se sulfanem (sirovodíkem) a mědí dá methan
- CS2 + 2 H2S + 8 Cu → CH4 + 4 Cu2S.
Jinou možností je reakce karbidu hliníku s vodou
- Al4C3 + 12 H2O → 3 CH4 + 4 Al(OH)3.
Laboratorně se dá připravit žíháním směsi octanu sodného s hydroxidem sodným(natronovým vápnem)
- CH3COONa + NaOH → CH4 + Na2CO3.
Vlastnosti
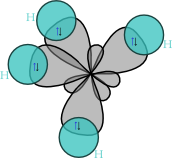
Molekula methanu má symetrii pravidelného čtyřstěnu (bodová grupa symetrie Td), v jehož těžišti se nachází uhlíkový atom a v jehož vrcholech se nacházejí vodíkové atomy. Díky této vysoké symetrii je celkově molekula methanu nepolární, přestože vazby H–C slabou polaritu vykazují.
Methan může reagovat explozivně s kyslíkem
CH4 + 2 O2 → CO2 + 2 H2O.
Bod samozážehu je sice velmi vysoký (595 °C, teplota vznícení při koncentraci 8,5 % je 537 °C), ale stačí např. elektrická jiskra nebo otevřený plamen a směs methanu se vzduchem může být přivedena k výbuchu (minimální iniciační energie je 0,28 mJ). Přitom meze výbušnosti jsou značně velké, od 4,4 do 15 objemových procent. Proto je nezbytně nutné průběžně sledovat koncentraci methanu (důlního plynu) v uhelných dolech, aby se předešlo katastrofám. Podobně prudce může methan reagovat i s plynným chlorem, je-li reakce iniciována prudkým zahřátím. Za normální teploty probíhá pomalu čtyřstupňově za vzniku chlorovaných derivátů methanu
- CH4 + Cl2 → CH3Cl + HCl,
- CH3Cl + Cl2 → CH2Cl2 + HCl,
- CH2Cl2 + Cl2 → CHCl3 + HCl,
- CHCl3 + Cl2 → CCl4 + HCl.
Podobně reaguje i s jinými halogeny. Jinak je málo reaktivní.
- Dokonalé hoření methanu
- CH4 + 2O2 → CO2 + 2H2O
- Nedokonalé hoření methanu
- CH4 + O2 → 2H2O + C, nebo
- 2CH4 + 3O2 → 4H2O + 2CO
Výskyt v přírodě
Methan se přirozeně vyskytuje na Zemi:
- v atmosféře, kam se dostává zejména jako produkt rozkladu látek biogenního původu (bioplyn), nebo jako produkt metabolismu velkých přežvýkavců, také z termitišť a z rýžovišť.
- v podzemí:
- jako hlavní složka zemního plynu
- jako součást důlního plynu v dolech
- rozpuštěný v ropě
- rozpuštěný ve vodě některých jezer, zvláště v Africe (např. jezero Kivu mezi Rwandou a Kongem)
- tvoří bublinky pod ledem rozmrzajícího permafrostu, například na Sibiři

Přítomnost ve vesmíru
Ve vesmíru byl nalezen v plynných mračnech v mezihvězdném prostoru.
Dále je obsažen v atmosférách velkých planet (Jupiter, Saturn, Uran a Neptun) sluneční soustavy. V pevném stavu je součástí tzv. ledových měsíců velkých planet a tvoří zřejmě nezanedbatelnou část hmoty transneptunických těles, případně je vysrážen ve formě ledu nebo jinovatky na jejich povrchu (např. Pluto). Byl také prokázán v komách komet.
Původ na Zemi
Na Zemi pochází asi 90 % metanu z produkce živých organismů, menší část vzniká při geologických aktivitách (např. tavením magmatu). Mezi přírodní zdroje patří mokřady (hnilobné procesy), lesy, mořské ekosystémy a také mikroorganismy v trávicím ústrojí živočichů (například archea v trávicím traktu skotu). Dalším zdrojem je těžba a spalování fosilních paliv, zemědělství (chov skotu) a skládky.
Podle studie z Institutu pro arktický a alpinský výzkum z roku 2024 jsou za růst koncentrace metanu v atmosféře Země v posledních letech zodpovědné mikroorganismy a nikoliv fosilní paliva. Původně bylo odhadováno, že fosilní zdroje mohou až za 30 % produkce, což studie zpochybňuje na základě obsahu izotopu uhlíku 13C. Zda zvýšení produkce metanu z mikrobiálních zdrojů je přírodního původu nebo důsledek lidské činnost, zatím není jasné.
Ve vesmíru však bez dalších podkladů nelze původ metanu prokázat. Zprávy některých médií, které z objevu metanu usuzují na existenci života ve vesmíru, jsou proto považovány za nepodložené.
Použití

Hlavní oblastí použití methanu je energetika, kde slouží ve směsi s jinými uhlovodíky jako plynné palivo. V automobilové dopravě představuje jednu z pohonných látek, pod označením CNG(Compressed Natural Gas), stlačený zemní plyn, jehož hlavní složku tvoří právě methan.
Methan je spolu s kyslíkem používán jako palivo pro raketové motory vesmírné lodi Starship.
V chemickém průmyslu se používá především k výrobě oxidu uhličitého dokonalým spalováním se vzduchem a při nedokonalém spalování k výrobě sazí používaných jako plnidlo a barvivo v gumárenském průmyslu. Pyrolýzou (tepelným rozkladem) za nepřístupu vzduchu se vyrábí ethyn (acetylen) a vodík.
Ekologické účinky



Vzhledem k tomu, že methan silně absorbuje infračervené záření, patří mezi významné skleníkové plyny zvyšující teplotu zemské atmosféry (je přibližně 20krát účinnější než oxid uhličitý, ale jeho obsah v atmosféře je oproti tomu asi 200krát menší než u oxidu uhličitého: 0,0002 % methanu a 0,04 % oxidu uhličitého, takže jeho vliv je přibližně 10krát menší). Metan se v atmosféře rozpadá během 10 až 12 let, takže jeho působení je sice intenzivnější než CO2, ale krátkodobější.
Produkují ho (prostřednictvím mikrobů) hlavně mokřady, dále hospodářská zvířata a v menší míře průmysl a skládky. Významným producentem jsou ale i jezera a fjordy. Byly objeveny i další zdroje: mořští mlži, či některé ledovce. Produkují ho i stromy. Zhruba polovina emisí methanu je z vodních ekosystémů. Studie dříve uvažovaly, že vlivem globálního oteplování se bude methan uvolňovat i z oceánu či tundry; nejnovější výzkumy však ukazují, že tomu tak být nemusí. Uvolňování metanu se také nadhodnocovalo
Methan je v atmosféře oxidován především působením hydroxylových radikálů. Dosavadní scénáře budoucího vývoje klimatu vycházejí z představy, že spolu s nárůstem koncentrace metanu bude v množství hydroxylových radikálů v atmosféře ubývat. Dlouhodobé sledování troposféry podalo důkaz, že koncentrace radikálu OH neklesají. Jeho molekuly opětovně vznikají působením slunečního záření. Jedním zdrojem jsou oxidy dusíku, druhým pak vodní páraa ozon za přispění ultrafialového záření v nižších vrstvách atmosféry.
| Methan | |
|---|---|
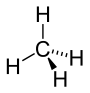
Strukturní vzorec
|
|

Tyčinkový model
|
|

Kalotový model
|
|
| Obecné | |
| Systematický název | methan |
| Triviální název | bahenní plyn |
| Ostatní názvy | metan |
| Sumární vzorec | CH4 |
| Vzhled | bezbarvý plyn |
| Identifikace | |
| Registrační číslo CAS | 74-82-8 |
| EC-no (EINECS/ELINCS/NLP) | 200-812-7 |
| Indexové číslo | 601-001-00-4 |
| Vlastnosti | |
| Molární hmotnost | 16,042 6 g/mol |
| Teplota tání | −182,5 °C |
| Teplota varu | −161,6 °C |
| Hustota | 0,676 kg/m3 (plyn, 21 °C, 1 013 hPa) 0,422 62 g/cm3(kapalina, −161,6 °C, 1 013 hPa) |
| Kritická teplota Tk | −82,7 °C |
| Kritický tlak pk | 4,596 MPa |
| Rozpustnost ve vodě | 0,22 mg/l (20 °C) |
| Struktura | |
| Dipólový moment | 0 |
| Bezpečnost | |
 GHS02 Nebezpečí |
|
| H-věty | H220 |
| R-věty | R12 |
| S-věty | (S2) S9 S16 S33 |
| NFPA 704 |
 4
1
0
|
| Teplota vzplanutí | −188 °C |
| Teplota vznícení | 600 °C |
| Meze výbušnosti | 5–15 % |
|
Není-li uvedeno jinak, jsou použity
jednotky SI a STP (25 °C, 100 kPa). |
|